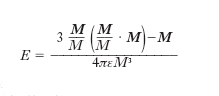Dipolo
Enciclopedia on line
Sistema costituito da due enti identici ma di diversa polarità.
Fisica
D. elettrico
Sistema costituito da due cariche puntiformi, di eguale valore q e di segno opposto, a distanza δ molto piccola rispetto a ogni altra lunghezza che compaia nel problema in esame; il momento del d. è il vettore M, di modulo qδ, diretto dalla carica negativa a quella positiva. Unità di misura del momento di d. elettrico è, nel SI, il coulomb per metro (C·m). Tale sistema genera nello spazio circostante un campo elettrico, d’intensità
essendo ε la costante dielettrica assoluta del mezzo, supponendo di usare il SI, e r la distanza orientata dal d. al punto che si considera. In un campo elettrico uniforme, di intensità E*, il d. è soggetto a una coppia di forze il cui momento vale M×E*. Come si dimostra, un sistema di cariche è assimilabile a un d. se la somma algebrica delle cariche è nulla e se la distribuzione delle cariche non ha un centro di simmetria: è il caso, per es., delle molecole a legame eteropolare (H2O, NaCl ecc.).
D. magnetico
Con ottima approssimazione è un magnete permanente a sbarra, piuttosto allungato (in concreto, il cosiddetto ago magnetico). Se un d. magnetico è immerso in un campo di induzione magnetica B, esso è soggetto a una coppia di forze il cui momento vale M×B, dove M è il momento magnetico del d. I circuiti percorsi da corrente sono assimilabili a d. magnetici, nel senso che a distanze molto grandi rispetto alle dimensioni di un circuito, il campo da questo generato è identico a quello generato da un d. di opportuno momento. Precisamente, un circuito, per es., una spira, delimitante una superficie di area S e percorso da corrente di intensità i è assimilabile a un d. il cui momento è dato da M=μ i S n, essendo μ la permeabilità magnetica del mezzo e n il versore della normale alla superficie anzidetta, orientato nel verso secondo il quale avanzerebbe una vite che ruotasse nel verso di circolazione della corrente. Per il fatto di essere assimilabili a minuscoli circuiti percorsi da corrente, gli elettroni orbitanti intorno a un nucleo atomico hanno un momento magnetico; indipendentemente dal moto di rivoluzione intorno al nucleo, gli elettroni (ed altre particelle elementari, per es. i protoni) sono dotati di un momento magnetico intrinseco come se essi fossero animati da un moto di rotazione (momento di spin). Il momento magnetico complessivo di un atomo o di una molecola è il risultante di tutti i momenti elementari, orbitali e di spin, dei costituenti, e può risultare a seconda dei casi nullo oppure no; hanno momento magnetico nullo, per es., le molecole delle sostanze diamagnetiche. Su scala macroscopica, un corpo magnetizzato è caratterizzato da un momento magnetico. L’intensità del campo magnetico generato da un d. magnetico è formalmente analoga all’intensità del campo elettrico generato da un d. elettrico. L’unità di misura del momento di d. magnetico è il weber per metro (Wb·m); in particolare, l’unità di misura dei momenti magnetici di molecole, atomi e particelle elementari è il magnetone di Bohr, pari a 1,17·10–29 Wb·m.
D. elettromagnetico
Particolarmente importante è il caso in cui il valore del momento di un d. elettrico o di un d. magnetico cambi nel tempo. Come si dimostra, è indifferente trattare un sistema di questo tipo in termini di d. elettrico o di d. magnetico, poiché esso è caratterizzato da due momenti, uno elettrico l’altro magnetico, indissolubilmente legati uno all’altro e variabili nel tempo con uguale legge; in questo caso si ha un d. elettromagnetico, da cui si irradia tutt’intorno un campo elettromagnetico. Esempi di d. elettromagnetici sono l’oscillatore di Hertz e le antenne in mezz’onda, dette anche antenne a dipolo (➔ antenna).
Chimica
D. molecolari Una molecola, pur essendo globalmente neutra, è sede di un momento dipolare permanente quando il centro delle cariche positive dei nuclei e quello delle cariche negative degli elettroni non coincidono. Questa situazione si verifica quando le molecole sono asimmetriche. Per es. le molecole del metano e del tetracloruro di carbonio, che hanno entrambe la struttura di un tetraedro con il carbonio al centro e gli altri atomi ai vertici, sono prive di momento dipolare, mentre i cloroderivati non completamente sostituiti del metano sono sede di un dipolo. Questo si rappresenta con un vettore avente la direzione della retta che passa attraverso i due centri di carica e sperimentalmente si determina attraverso una misura della dipendenza della costante dielettrica della sostanza dalla temperatura.
© Istituto della Enciclopedia Italiana - Riproduzione riservata